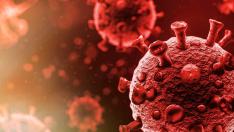
След повече от година в положение на COVID-19 пандемия, през последните месеци започнаха да се установяват все по-голям брой нови щамове на вируса, които проявяват по-висока заразност и инвазивни способности за „прескачане“ на имунната защита на организма.
В ново проучване, публикувано в списанието Cell, изследователи от Германия установяват, че новите варианти B.1.1.7 (или т.нар. Великобритански вариант), B.1.351 (Южно-Африкански) и P.1 (Бразилски) варианти не показват по-лесно навлизане в клетката гостоприемник. Екипът установява още, че Южно-Африканският и Бразилският варианти имат потенциала да избягват терапевтични антитела или антитела индуцирани след естествено боледуване или ваксинация, пише Puls.bg.
Във Великобритания, B.1.1.7 вариантът на вируса се появява с различни мутации на т.нар. spike гликопротеин – N50Y1 мутацията, 69/70 делеция, E484K, което може да промени неутрализирането от моноклонални антитела; както и P681H, който беше установен за първи път през декември 2020 и от тогава, до сега, достигна до много страни. Скорошни проучвания показват, че тези варианти могат да се разпространяват по-бързо и да са свързани с по-висока смъртност.
Междувременно, в Южна Африка се появи нов вариант – B.1.351, който споделя някои общи мутации с B.1.1.7 вариантът, като E484K и N501Y.
P.1 вариантът на вируса беше установен за първи път у бразилски туристи, тествани в Япония. Щамът има 17 уникални мутации, включително три в рецептор-свързващия домен (receptor-binding domain, RBD) на т.нар. spike protein. Не е ясно дали антитяло респонсът у ковалесцентни пациенти предпазва срещу реинфекция с новите варианти.
В проучването, екипът изучава как S протеините на B.1.1.7, B.1.351 и P.1 вариантите водят до фузия с човешките клетки и установяват, че S протеинът не успява да медиира фузия с таргетни клетки, които експресират само ангиотензин-конвертиращ ензим 2 (ACE2), но успешно се фузират с клетки, които ко-експресират ACE2 и TMPRSS2. По този начин достъпът може да бъде блокиран разтворими ACE2 протеазни инхибитори срещу TMPRSS2 и инхибитори на мембранната фузия.
Екипът установява още, че моноклонални антитела, които бяха одобрени в условия на спешност (EUA – emergency use authorization) за лечение на COVID-19 тежки инфекции, не успяват напълно или частично да неутрализират S протеините на варианти B.1.351 и P.1. Въпреки че като взаимодействие с клетките на гостоприемника и навлизането в тях, различните щамове не се различават сигнификантно, то значителни различия в податливостта към антитяло-медиираната неутрализация се нбалюдавали. Проучването показва още, че навлизането на същите два варианта в клетките на гостоприемника, с помощта на S протеинът, частично се инхибира от лекарството Casirivimab, a комбинирането му с Imdevimab е още по-ефективно. Този коктейл от моноклонални антитела е одобрен за използване в условия на спешност (REGN-COV2).
Оказва се също, че вариантите били по-слабо инхибирани и от рековалесцентна плазма, както и серум от хора, които са ваксинирани с иРНК BNT162b2 ваксината срещу COVID-19. Екипът изказва заключение, че B.1.351 и P.1 вариантите са устойчиви на неутрализиращи антитела и това може да се окаже заплаха към световния стремеж за масова ваксинация. Различна е ситуацията за B.1.1.7 щамът, който може ефективно да бъде инхибиран от антитела, получени след естествено боледуване или ваксинация.







 Под горещото слънце на Гиза: Маратон събра мнозина край пирамидите (СНИМКИ)
Под горещото слънце на Гиза: Маратон събра мнозина край пирамидите (СНИМКИ)  Операция "Паяжина" на Украйна е увековечена в монета с Троянски кон в Русия (+СНИМКИ)
Операция "Паяжина" на Украйна е увековечена в монета с Троянски кон в Русия (+СНИМКИ)  Ужасяващи кадри на агресия към куче в Троян: Задържаха 22-годишен насилник
Ужасяващи кадри на агресия към куче в Троян: Задържаха 22-годишен насилник  Банско откри ски сезона с атрактивна програма
Банско откри ски сезона с атрактивна програма 
 Лунната почва може да съдържа следи от земната атмосфера
Лунната почва може да съдържа следи от земната атмосфера  Антитела, проектирани от изкуствен интелект, ще бъдат тествани на хора
Антитела, проектирани от изкуствен интелект, ще бъдат тествани на хора  Признаци за бъдеща катастрофа в Антарктида
Признаци за бъдеща катастрофа в Антарктида  Разкриха влиянието на Марс върху климата на Земята
Разкриха влиянието на Марс върху климата на Земята 
 От други ъгли: Вижте как Гасиев нокаутира Пулев + ВИДЕО
От други ъгли: Вижте как Гасиев нокаутира Пулев + ВИДЕО  Кобрата каза защо яде бой от Гасиев
Кобрата каза защо яде бой от Гасиев  Бат' Венци: ЦСКА 1948 е като Дейвид Копърфийлд. Крив отбор!
Бат' Венци: ЦСКА 1948 е като Дейвид Копърфийлд. Крив отбор!  Легенда разкри голям проблем в ЦСКА
Легенда разкри голям проблем в ЦСКА 
 Любовен хороскоп за 15 – 21 декември
Любовен хороскоп за 15 – 21 декември  Как да изберем рокля според типа фигура
Как да изберем рокля според типа фигура  TASH SULTANA - за първи път в България на 11 август 2026
TASH SULTANA - за първи път в България на 11 август 2026  Вкусни питки за Бъдни вечер
Вкусни питки за Бъдни вечер 
 Чрез микропластмасата се разпространяват опасни бактерии
Чрез микропластмасата се разпространяват опасни бактерии  Клиника по неврохирургия в УМБАЛ „Св. Иван Рилски“ отпразнува своята 20-годишнина
Клиника по неврохирургия в УМБАЛ „Св. Иван Рилски“ отпразнува своята 20-годишнина  Защо се будим малко преди алармата?
Защо се будим малко преди алармата?  Наследствена ли е шизофренията?
Наследствена ли е шизофренията? 
 дава под наем, Четиристаен апартамент, 200 m2 София, Овча Купел, 1100 EUR
дава под наем, Четиристаен апартамент, 200 m2 София, Овча Купел, 1100 EUR  дава под наем, Тристаен апартамент, 120 m2 Варна, Генералите, 600 EUR
дава под наем, Тристаен апартамент, 120 m2 Варна, Генералите, 600 EUR  дава под наем, Тристаен апартамент, 64 m2 Варна, Парк Владислав Варненчик, 435 EUR
дава под наем, Тристаен апартамент, 64 m2 Варна, Парк Владислав Варненчик, 435 EUR  дава под наем, Двустаен апартамент, 60 m2 Варна, Аспарухово, 375 EUR
дава под наем, Двустаен апартамент, 60 m2 Варна, Аспарухово, 375 EUR 











 Представителите на Фед са разделени за рисковете за американската икономика през 2026 г.
Представителите на Фед са разделени за рисковете за американската икономика през 2026 г.  Под горещото слънце на Гиза: Маратон събра мнозина край пирамидите (СНИМКИ)
Под горещото слънце на Гиза: Маратон събра мнозина край пирамидите (СНИМКИ)  Китай налага равносметка в Европа, като търговията става реална заплаха
Китай налага равносметка в Европа, като търговията става реална заплаха  10 много яки функции на новия Mercedes GLB
10 много яки функции на новия Mercedes GLB  Френски маникюр за празниците – от подаръци до снежинки
Френски маникюр за празниците – от подаръци до снежинки  4 зодии, които ще излекуват разбитото си сърце през зимата
4 зодии, които ще излекуват разбитото си сърце през зимата
Коментари